Oda sıcaklığında sodyum iyon pillerin yeniden canlanması
Yer kabuğundaki bol miktardaki sodyum (Na) rezervleri ve sodyum ile lityumun benzer fizikokimyasal özellikleri nedeniyle, sodyum bazlı elektrokimyasal enerji depolama, büyük ölçekli enerji depolama ve şebeke gelişimi için önemli umut vaat etmektedir. Örneğin, sabit ve mobil uygulamaların başarılı ticari örnekleri olan Na/NiCl2 sistemlerine dayalı yüksek sıcaklıkta sıfır emisyonlu pil araştırma faaliyet hücreleri ve yüksek sıcaklıktaki Na-S hücreleri, sodyum bazlı şarj edilebilir pillerin potansiyelini zaten göstermiştir. Bununla birlikte, yaklaşık 300 °C'lik yüksek çalışma sıcaklıkları güvenlik sorunlarına neden olur ve sodyum iyon pillerin (SIB'ler) gidiş-dönüş verimliliğini azaltır. Oda sıcaklığındaki (RT) SIB'ler bu nedenle yaygın olarak LIB'lere en umut verici alternatif teknoloji olarak kabul edilmektedir.
Pillerin son 200 yıllık tarihi boyunca, SIB'ler üzerine araştırmalar, LIB gelişimiyle yan yana hararetle yürütüldü. TiS2'nin lityum için elektrokimyasal aktivitesi ve enerji depolamaya yönelik fizibilitesi ilk olarak 1970'lerde ortaya konmuştur. Bu keşfin ardından Na iyonlarının TiS+2'ye eklenebilme yeteneği 1980'lerin başında fark edildi. Grafitin LIB'ler için düşük maliyetli ve orta kapasiteli bir anot malzemesi olarak keşfedilmesi ve sodyum iyonlarının birbirine eklenmesindeki başarısızlıkla birlikte, 1990'larda hızlı LIB gelişimi meydana geldi ve sodyum kimyasındaki büyümenin yerini aldı. Daha sonra, 2000 yılında, grafitteki Li'ninkine benzer bir enerji kapasitesi sağlayacak olan sert karbonda (HC) sodyum depolamanın mevcudiyeti, SIB'lere yönelik araştırma ilgisini yeniden canlandırdı.
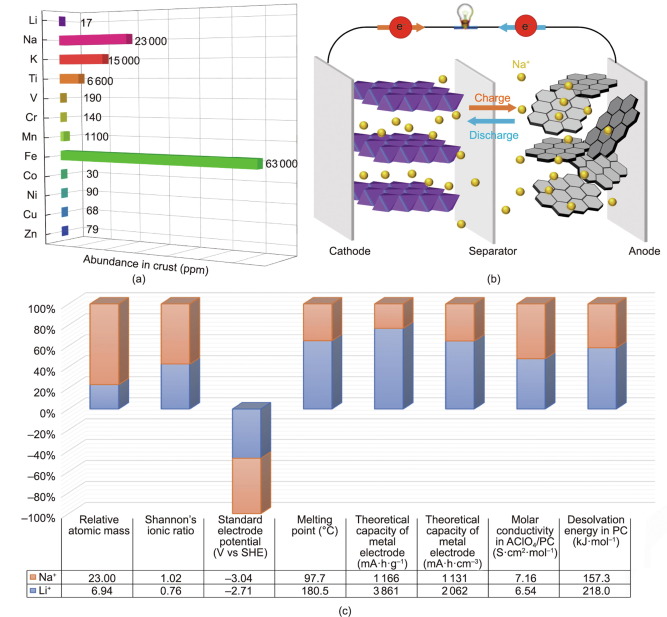
Sodyum-iyon pil ile Lityum-iyon pilin karşılaştırılması
SIB'lerin yeniden canlanması, lityum rezervlerinin bulunmamasından kaynaklanan giderek artan baskı ve buna karşılık gelen maliyet artışıyla birleştiğinde, LIB'ler için tamamlayıcı bir strateji sağlıyor. SIB'ler, yenilenebilir enerji teknolojilerinin artan yaygınlığını karşılama çabasında, malzeme bilimindeki temel başarılarla birlikte artan araştırma ilgisi kazanmıştır. SIB'lerin hücre bileşenleri ve elektrokimyasal reaksiyon mekanizmaları, birinde Na, diğerinde Li olan yük taşıyıcısı dışında temel olarak LIB'lerinkilerle aynıdır. SIB malzeme kimyasındaki hızlı genişlemenin ana nedeni, iki alkali metal arasındaki fizikokimyasal özelliklerdeki paralelliklere atfedilir.
Birincisi, yük taşıyıcı olarak Na görev yapmasına rağmen, SIB'lerin çalışma prensipleri ve hücre yapısı ticari LIB'lerinkine benzer. Tipik bir SIB'de dört ana bileşen bulunur: bir katot malzemesi (genellikle Na içeren bir bileşik); bir anot malzemesi (Na içermesi şart değildir); bir elektrolit (sıvı veya katı halde); ve bir ayırıcı. Şarj işlemi sırasında, tipik olarak katmanlı metal oksitler ve polianyonik bileşikler olan katotlardan sodyum iyonları çıkarılır ve daha sonra anotlara eklenir, bu sırada akım harici bir devre üzerinden ters yönde ilerler. Na boşalırken anotları terk eder ve "sallanan sandalye prensibi" olarak adlandırılan bir süreçte katotlara geri döner. Bu benzerlikler SIB teknolojisinin ön anlaşılmasını ve hızlı büyümesini sağlamıştır.
Dahası, Na'nın daha büyük iyon yarıçapı kendi avantajlarını da beraberinde getirir: elektrokimyasal pozitifliğin artan esnekliği ve polar çözücülerde azalan de-solvasyon enerjisi. Li ve geçiş metali iyonları arasındaki iyonik yarıçaptaki daha büyük boşluk genellikle malzeme tasarımının esnekliğinin başarısız olmasına yol açar. Buna karşılık, sodyum bazlı bir sistem, lityum bazlı bir sisteme göre daha esnek katı yapılara olanak tanır ve çok büyük iyonik iletkenliğe sahiptir. Tipik bir örnek, Na ara katmanının mükemmel boyuta ve yüksek iletkenliğe sahip olduğu β-Al2O3'tür. Farklı M+x+ istifleme şekillerine sahip daha katmanlı geçiş metali oksitleri, sodyum bazlı bir sistemde kolaylıkla gerçekleştirilebilir. Benzer şekilde, sodyum iyonik iletken (NaSICON) ailesi için bilinen çok çeşitli kristal yapılar, lityum analoglarınınkinden çok daha karmaşıktır. Daha da önemlisi, NaSICON bileşiklerinde, lityum iyonik iletken (LiSICON) bileşiklerindeki iyonik iletkenliği çok aşan çok daha yüksek bir iyonik iletkenliğe izin verilebilir.
Son olarak, farklı aprotik polar çözücülerle yapılan sistematik araştırmalar, Na'nın daha büyük iyon yarıçapının daha zayıf bir desolvasyon enerjisine neden olduğunu göstermiştir. Her ikisi de aynı değerliliğe sahip olduğunda, daha küçük Li, çekirdek çevresinde Na'ya göre daha yüksek bir yüzey yük yoğunluğuna sahiptir. Bu nedenle Li, polar çözücü moleküllerle daha fazla elektron paylaşarak termodinamik olarak stabilize edilir. Yani Li, bir Lewis asidi türü olarak sınıflandırılabilir. Sonuç olarak, oldukça polarize Li için nispeten yüksek bir desolvasyon enerjisine ihtiyaç vardır ve bu da Li'nin sıvı halden (elektrolit) katı duruma (elektrot) taşınmasıyla nispeten büyük bir transfer direncinin indüklenmesine yol açar. Desolvasyon enerjisi, sıvı/katı arayüzünde meydana gelen transfer kinetiği ile yakından ilişkili olduğundan, nispeten düşük desolvasyon enerjisi, yüksek güçlü SIB'lerin tasarımında önemli bir avantajdır.